我国临床前CRO行业发展现状分析
临床前 CRO 主要包括新药发现、先导化合物和活性药物中间体的合成及工艺开发、制剂研究、药效评价、药代动力学和安全性评价研究服务等工作,各阶段工作的研究方法技术创新难度较大,要求 CRO 企业具有丰富的经验积累及较强的技术优化能力。
一、我国临床前 CRO发展现状
药品市场全球化能够实现药物研发技术、药物价格的全球融通,同时促进药品市场内部的良性竞争。无论是对于想要国际化的内资药企还是想要拓宽国际市场的海外巨头,具备国际资质认证的医药外包企业都将是这些药企的首要选择。
药物临床前研究作为医药研发、生产中的重要一环,各国都有严格的准入和数据认可标准。美国FDA对于GLP 检查、欧洲经济合作与发展组织OECD对GLP的认证(检查)有着极为严格的质量要求,在通过相应检查的同时,企业还将出具相应的研究报告才能顺利被美国FDA和OECD相关成员国认可。因此具备国际GLP资质认证的临床前CRO企业出具的研究数据可以由客户选择进行多地申报,从而获得更多的客户青睐。
CRO与企业合作模式有传统模式、创新型模式、结果导向模式和风险共担模式等。根据CRO与药企间的合作方式,其商业模式可分为四种:“一手交钱,一手交货”的传统模式;“里程碑”付费的创新型模式;“赏罚分明”的结果导向模式;“共担风险,共享收益”的风险共担模式。
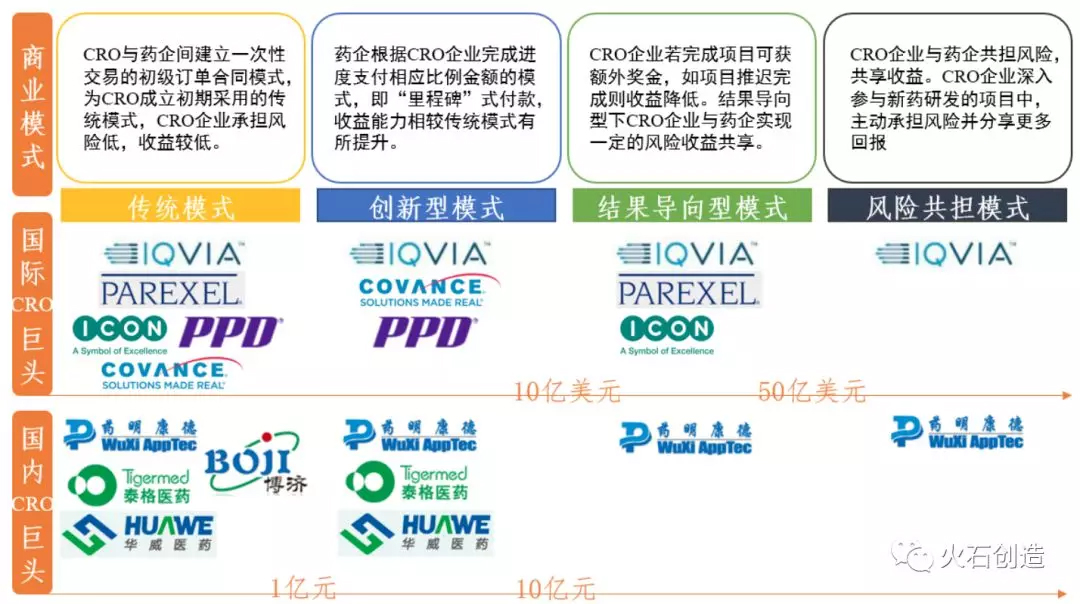
图1 CRO的四种商业模式
资料来源:中信证券、火石研究院整理
二、临床前新药研发服务内容和流程
临床前新药研发服务内容包括药物发现、药学研究和临床前研究。药物发现研发服务项目包括蛋白靶标验证、结构生物学、化学合成、化合物活性筛选及优化;药学研究包括原料药与制剂工艺研究、质量标准和稳定性研究;临床前研究包括药效学、药代动力学、毒理学安全性评价研究等。

图2 生物医药临床前CRO服务的主要内容
临床前 CRO 主要包括新药发现、先导化合物和活性药物中间体的合成及工艺开发、制剂研究、药效评价、药代动力学和安全性评价研究服务等工作,各阶段工作的研究方法技术创新难度较大,要求 CRO 企业具有丰富的经验积累及较强的技术优化能力。

图3 新药研发技术流程及学科分析
三、临床前CRO服务模式及流程
临床前CRO服务模式通常有产品定制模式、设计研发模式和联合攻关模式3个主要合作模式。

表1 临床前CRO服务模式
临床前CRO服务的业务流程包括项目洽谈、项目评估、签署合同、设计方案、试验实施、项目交付与售后服务等关键环节。

图4 临床前CRO服务流程
四、我国临床前CRO企业发展策略
随着创新药政策宽松,国际 CRO 需求转移等宏观环境变化,成立较早的药明康德、睿智化学、泰格医药、博济医药等本土 CRO 公司已占据国内行业领先梯队。在临床前研究方面,药明康德、康龙化成、昭衍新药、美迪西等主要临床前 CRO 企业具备直接参与国际竞争的实力。

表2 典型CRO企业的临床前研究实力情况(部分)
昭衍新药、中美冠科、美迪西和益诺思(国家上海新药安全评价研究中心)等多家专注于临床前服务的企业凭借多年业务经验,积累了许多长期合作客户,并通过高质量动物模型、动物实验的提供维持了自身的长期竞争优势。

表3 国内部分专注于临床前服务的企业发展情况
五、小结
随着我国 GLP认证制度的不断完善和新药研发数量的增加,我国临床前 CRO 技术水平也逐步和国际接轨。我国拥有丰富的人才资源和实验资源储备,政策利好,充分具备持续发展条件,而创新方面,我国生物医药创新热潮兴起,直接带动了临床前 CRO 行业快速发展。
大型跨国 CRO 机构进入国内,并且资源网络丰富、技术积累雄厚、业务覆盖面广,本土CRO企业面临直接竞争和挑战,未来在研发投入、研发意识方面还需要进一步提高,应充分借助大数据及AI等新技术,完成医药企业和服务方的供需智能匹配,缩短创新周期,提升创新效能,最终实现弯道超车。
来源:火石创造 作者:雷晗






