北京大学在人工智能助力时间分辨冷冻电镜重建蛋白质动力学调控方面取得突破性进展
北京大学物理学院凝聚态物理与材料物理研究所、人工微结构和介观物理国家重点实验室、国家生物医学成像科学中心、北大-清华生命科学联合中心、定量生物学中心毛有东教授团队利用自主研发的深度学习高精度四维重建技术,发展并应用时间分辨冷冻电镜,阐明了原子水平人源蛋白酶体动力学调控和构象重编程机制。2022年4月27日,相关研究成果以《时间分辨冷冻电镜解析人源蛋白酶体在USP14调控下的变构》(“USP14-regulatedallostery of the human proteasome by time-resolved cryo-EM”)为题,在线发表于国际顶级学术期刊《自然》(Nature)。
同期,研究人员、审稿人和Nature编辑团队联合,在研究简报(Research Briefing)专栏在线发表了题为《人体蛋白质降解机制的控制揭示》(“Control of human protein-degradation machinery revealed”)的推介文章,其中审稿人评价“该工作是一项重大研究,终于在原子水平解决了USP14活化和其调控蛋白酶体功能的机制问题”;Nature编辑团队指出“这一工作通过时间分辨冷冻电镜,结合功能分析……呈现了蛋白质降解过程中USP14和蛋白酶体的构象连续体”。这是首次将人工智能四维重建技术应用于大幅提升时间分辨冷冻电镜分析精度,针对重大疾病靶蛋白复合体,实现原子水平功能动力学观测的国际领先原创成果,展示了一类新型的蛋白质复合动力学研究范式。
蛋白质降解调控是极其重要的基本生物化学过程,在细胞周期、信号转导、免疫响应、基因调控、新陈代谢、神经退行、癌症肿瘤、病毒感染以及蛋白毒性响应等主要细胞分子过程中发挥着关键的调控作用。在真核细胞中,绝大部分胞内蛋白都是通过泛素蛋白酶体途径(Ubiquitin-proteasome pathway),经过泛素化标记被蛋白酶体全酶降解的。2004年,Aaron Ciechanover,Irwin Rose和AvramHershko三位科学家因“对该泛素化通路介导蛋白质降解的历史性发现”被授予诺贝尔化学奖。蛋白酶体全酶,又称为26S proteasome,是由中间一个圆柱形20S核心颗粒和两端覆盖的一个或两个19S调节颗粒组成。19S包含一个环形异源六聚体马达——AAA-ATPase,通过多个协同ATP水解模式调控蛋白酶体降解泛素化底物。蛋白酶体功能紊乱与人体多种疾病相关,如癌症、神经退行性疾病和免疫疾病等。蛋白酶体是美国食品药品监督管理局(FDA)批准的多种治疗癌症的上市小分子药物的直接靶标。在正常细胞中,蛋白酶体的功能受到多个水平的严格调控。去泛素化酶USP14是最主要的蛋白酶体调控分子,被认为是一个潜力巨大的治疗癌症和神经退行性疾病的重要靶标,其小分子抑制剂曾进入过美国一期临床研究,但围绕USP14功能机制的一系列悬而未决的关键问题极大地限制了其靶向药物分子的开发和临床应用。USP14通过结合26S而被激活,然后以毫秒的时间尺度剪切底物上的泛素链;但其如何被蛋白酶体激活并调控蛋白酶体功能,一直是全球研究机构和生物制药领域期待解决的关键科学问题。
生命分子机器通过高度复杂的非平衡动力学过程和结构变化来实现其特殊功能,这一过程进而受到各种复杂分子间相互作用的精准调控。如何在原子水平直接观察天然态超大分子机器的功能态动力学过程,给现有的原子结构动态分析技术提出了空前挑战。
毛有东教授团队长期致力于发展基于冷冻电镜的动力学重建方法,围绕蛋白酶体、炎症小体等具有重大临床应用前景的靶点系统的结构功能、动力学机制和靶向调控分子设计深入开展前沿交叉研究:2016年,在《美国国家科学院院刊》(PNAS)上报道了人源蛋白酶体基态的3.6 Å冷冻电镜结构及其他三个亚纳米分辨构象,并首次发现一个亚稳态构象的核心颗粒物转运通道处于开放状态(PNAS 2016; 113: 12991-12996);2017年,利用冷冻电镜解析高分辨率蛋白酶体19S调控复合体在结合组装伴侣p28的自由态的三维结构,阐释了组装伴侣蛋白Gankyrin/p28在蛋白酶体组装过程中构象选择的组装机理(Molecular Cell 2017; 67: 322-333);2018年4月,在《自然·通讯》(Nature Communications)上报道了6个ATPγS结合状态下的26S蛋白酶体动态结构,包括三个核心颗粒复合物开放态对应的亚稳简并态近原子分辨(4~5 Å)结构(Nature Communications 2018, 9: 1360);2018年11月,在《自然》(Nature)上首次报道了人源蛋白酶体26S在降解底物过程中的七种中间态构象的高分辨(2.8~3.6Å)结构,在原子水平呈现了蛋白酶体和底物相互作用的动态过程,首次实现了对AAA-ATPase六聚马达分子内ATP水解全周循环的完整过程的原子水平观测(Nature 2019; 565: 49-55)。这一系列工作揭示了蛋白酶体的原子架构、组装原理和降解泛素化底物的动力学基本规律。
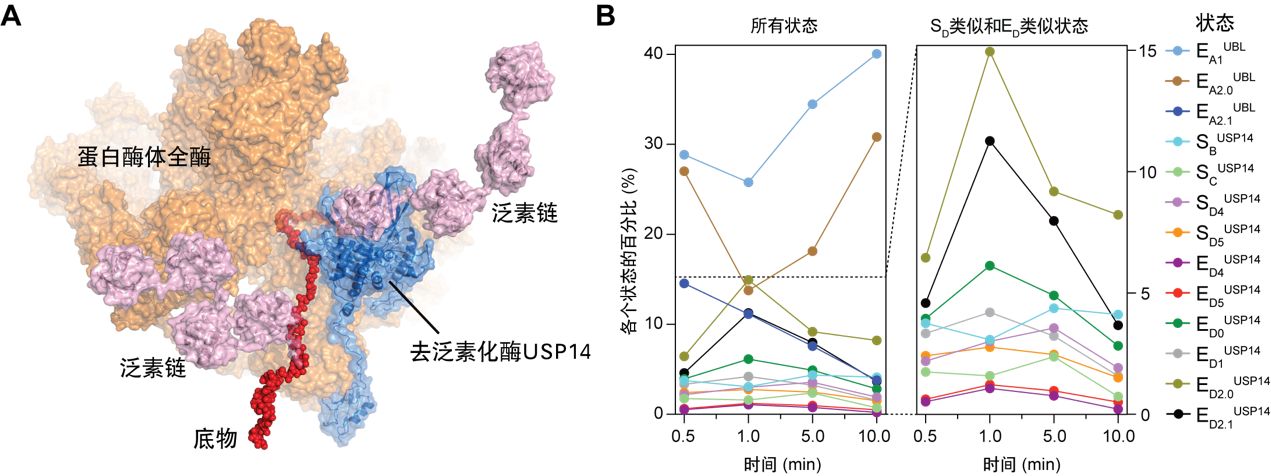
(A) USP14调控下蛋白酶体复合体降解多泛素化底物的原子结构模型之一;(B) 时间分辨率冷冻电镜解析13种中间态的统计分布随蛋白质降解进程的时间演化(Youdong Mao, CC BY 4.0)
科学研究的过程总是艰难曲折,要克服的首要困难是“时间分辨”:蛋白酶体降解底物的过程很快,时间尺度在毫秒至秒之间,正常条件下,想要通过冷冻电镜技术捕获此过程的中间态结构非常困难,因此,首先要让这个过程慢下来。研究团队通过大量的条件摸索,重建反应动力学体系和优化反应条件,包括优化缓冲体系、反应温度等条件,优化出较为可行的实验方案,从而使得时间分辨冷冻电镜技术应用成为可能,最终获得了含时的45,193张USP14-26S复合体降解泛素底物过程中的冷冻电镜透射图样,挑取了3,556,806个USP14-26S-泛素底物复合体的颗粒图像。
接下来面临的极端挑战是“三维分类”,冷冻电镜捕获的复合体图像需要经过一系列的分类,将它们归为不同的构象类别,才能呈现出蛋白反应的动态过程。USP14结合到26S蛋白酶体后,使得降解底物的动力学过程更加复杂,想要在如此多的异构复合体颗粒图像中,鉴别出降解过程的各个时态的高分辨率非平衡构象,传统的三维分类方法是无法实现的。低精度的三维分类将导致低分辨的三维重建,从而无法获取原子水平的动力学信息,无法对含时的数据赋予自洽的动态变化的物理意义。研究团队结合经过数年自主开发的新型深度学习高精度三维分类和四维重建方法,捕获了USP14-26S复合体降解多泛素化底物过程的13种不同功能中间状态的高分辨率(3.0~3.6Å)非平衡构象,通过时间分辨冷冻电镜分析,重建了受控蛋白酶体的完整动力学工作周期,并结合分子生物学功能和基因突变研究,阐明了USP14和26S相互调控活性的原子结构基础和非平衡动力学机制。
研究发现USP14的活化同时依赖于泛素识别和蛋白酶体RPT1亚基的结合。出人意料的是,USP14通过别构效应,诱导蛋白酶体同时沿着两条并行状态转变路径发生构象变化;研究团队成功捕获到了底物降解中间状态向底物抑制中间状态的瞬时转化。在底物降解途径中,USP14活化变构地重编程AAA-ATP酶马达的构象景观(Conformational landscape)和统计分布,并刺激20S底物通道的打开,从而观察到底物持续转运过程的ATPase六聚马达非对称ATP水解和近乎完整的全周循环周期。USP14-ATPase的动态相互作用,使得ATPase马达底物识别与26S自身的去泛素化酶RPN11催化发生去耦合效应,并在26S的泛素识别、底物的起始易位和泛素链回收过程中引入三个调控检查点(动力学分岔点)。这些发现为USP14调节26S的完整功能周期提供了全新的高分辨见解,并为USP14靶向药物治疗发现奠定了极为重要的机制基础。
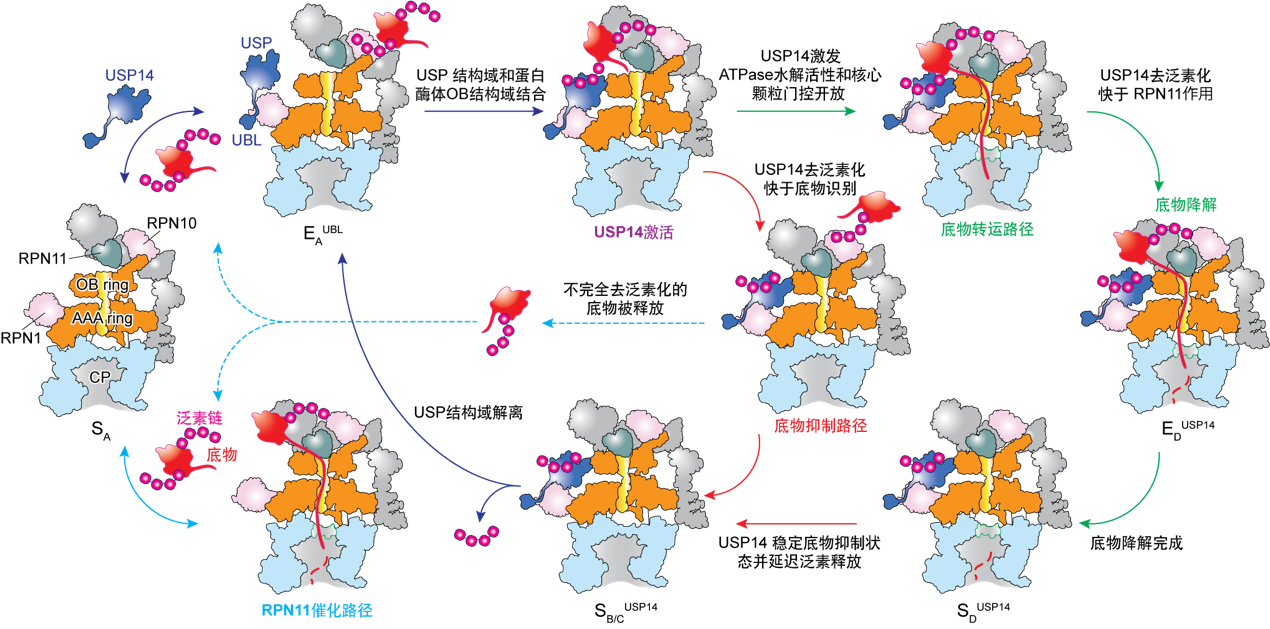
通过时间分辨冷冻电镜分析获取的USP14调控蛋白酶体底物降解的并行路径模型(Youdong Mao, CC BY 4.0)
北京大学“博雅”博士后张书文和北京大学物理学院2019级博士研究生邹士涛为论文的共同第一作者,毛有东为通讯作者。研究工作中的全部冷冻电镜数据在北京大学电子显微镜实验室和冷冻电镜平台上完成采集,大部分数据分析工作在北京大学高性能计算平台上完成。
上述研究工作得到北京市自然科学基金、国家自然科学基金、国家杰出青年科学基金,北大-清华生命科学联合中心等支持。
来源:北京大学


本文系作者 @TIMEDOO 原创发布在 肽度TIMEDOO。未经许可,禁止转载。




